СИНДРОМ ХРОНІЧНОЇ БАКТЕРІАЛЬНОЇ ІНТОКСИКАЦІЇ.
Повідомлення 5. КЛІНІЧНИЙ ДІАГНОЗ (продовження).
І.С.Марков, А.І.Марков
Клініка Вітацелл, Клініка Маркова (Київ)
Резюме. Метою дослідження було продовження вивчення клінічних проявів синдрому хронічної бактеріальної інтоксикації (СХБІ), викликаних дією дерматотропних, артроміотропних та офтальмотропних токсинів.
Дизайн дослідження як і раніше був клініко-діагностичним та включав визначення клінічних проявів такого досі невідомого захворювання, яке отримало назву синдром хронічної бактеріальної інтоксикації (СХБІ), що тривалий час проходило під маскою діагнозу ME/CFS. Дослідження носили проспективно-ретроспективний характер та були лонгітудинальними.
Стиль викладення матеріалу – розповідний, як і раніше не нудний.
Умови: дослідження були багатоцентровими та проведенні в амбулаторних умовах на базі 2-х спеціалізованих в галузі хронічних інфекційних захворювань клінік з повним обсягом лабораторних досліджень. Учасниками дослідження були усі пацієнти, які на протязі 2009-2020 років зверталися на консультацію до клінік зі скаргами, що відповідали діагнозу синдром хронічної втоми (CFS), який майже третині пацієнтів був встановлений раніше на попередніх етапах обстеження та лікування.
Результати. У Повідомленні 5 продовжено розгляд клінічних проявів синдрому хронічної бактеріальної інтоксикації у 4500 дітей та дорослих відповідно до таблиці 1, приведеною у Повідомленні 2, а саме клінічні симптоми та патологічні стани, викликані дерматотропними токсинами – бактеріальні токсикодермії, які спостерігали у 222/540 (41 %) дітей у віці до 3-х років, у 398/750 (53 %) – від 3-х до 7 років, у 392/870 (45 %) - від 7 до 14 років та у 889/2340 (38 %) дорослих. Ураження шкіри майже завжди було поєднаним з іншими симптомами СХБІ, хоча нерідко помітно домінувало у клінічній картині захворювання. До клінічних проявів СХБІ, викликаних артроміотропними токсинами, алгічні прояви яких з боку суглобів, хребта та м’язів частково були розглянуті раніше у Повідомленні 3, відносили реактивні артрити (РеА), які спостерігали у 770/4500 (17,1 %) хворих на СХБІ. Дорослих було 540/2340 (23 %), дітей шкільного віку – 157/870 (18 %) та у віці від 3-х до 7 років – 73/750 (9,7 %). Було встановлено, що РеА не були пов’язані з попередньо перенесеними гострими кишковими та статевими інфекціями, а також із хронічним статевим хламідіозом, а розвивалися на тлі хронічної бактеріальної інфекції в нирках - нефродисбактеріозу, рідше – маніфестного пієлонефриту, що призвело до розвитку СХБІ з домінуючим ураженням суглобів, яким хибно надавали інші діагнози. Частина бактеріальних токсинів при СХБІ мала офтальмотропну дію, з якою були пов’язані такі клінічні стани як токсичний кон’юнктивіт ендогенного походження, що спостерігали у 211/2340 (9 %) дорослих та 18/870 (2 %) дітей шкільного віку, токсичний увеїт ендогенного походження, який було встановлено 24/4500 (0,53 %) пацієнтам, ретробульбарний неврит зорового нерву, який спостерігали у 5/2340 (0,57 %) та тимчасова минуча диплопія, яка розвинулася у 7/2340 (0,3 %) дорослих. Встановлено, що майже у 100 % дітей та у 50-70 % дорослих з СХБІ була супутня хронічна стафілококова інфекція, первинне вогнище якої знаходилося у носоглотці, що привносило у клінічну картину захворювання типові для цієї інфекції додаткові клінічні симптоми. Наголошено, що у 63% дорослих пацієнтів та 73 % дітей на момент встановлення їм діагнозу СХБІ в них існував нефродисбактеріоз у «чистому» вигляді без усяких ознак запального процесу в нирках. Встановлено таку характерну клінічну обставину як існування моносимптомного СХБІ, який мав не просто домінуючий, а майже тільки один прояв, що треба було враховувати при встановлені відповідного діагнозу.
Висновки. Одними із типових клінічних проявів у недужих на СХБІ були симптоми та патологічні стани, пов’язані з дією дерматотропних, артроміотропних та офтальмотропних токсинів бактерій на тлі вогнища хронічної бактеріальної інфекції у нирках (нефродисбактеріозу).
Відомо: існування діагнозу міалгічний енцефаломієліт/синдром хронічної втоми (ME/CFS) з невизначеною етіологічною причиною.
Нове: вперше клінічно визначено та лабораторно підтверджено, що під маскою ME/CFS прихований досі невідомий синдром хронічної бактеріальної інтоксикації, який розвивається на тлі вогнища хронічної бактеріальної зазвичай локально безсимптомної інфекції у нирках, яке отримало назву нефродисбактеріозу. Вперше визначені клінічні прояви СХБІ, викликані дією дерматотропних, артроміотропних та офтальмотропних токсинів.
Ключові слова: синдром хронічної бактеріальної інтоксикації, нефродисбактеріоз, бактеріальні токсикодермії, реактивні та ревматоїдні артрити, офтальмотропні токсини, токсичний кон’юнктивіт, токсичний увеїт, міалгічний енцефаломієліт /синдром хронічної втоми (ME/CFS).
Друкується уперше.
Серед симптомів та захворювань, які були пов’язані з дією дерматотропних токсинів у хворих на СХБІ, треба окремо відзначити дуже часте пряме ураження шкіри з появою різноманітних варіантів дерматитів, які, незважаючи на різні назви, поєднувала одна загальна патогенетична причина: вони були викликані бактеріальними токсинами дерматологічної спрямованості. Бактеріальні токсикодермії частіше спостерігали у дітей: у віці до 3-х років – у 222/540 (41 %) випадках, у віці від 3-х до 7 років – у 398/750 (53 %), від 7 до 14 років – у 392/870 (45 %) та у 889/2340 (38 %) дорослих. Ураження шкіри майже завжди було поєднаним з іншими симптомами СХБІ, хоча нерідко помітно домінувало у клінічній картині захворювання.
Вікіпедія трактує токсикодермію як «гостре запалення шкірних покривів під впливом речовин, що потрапляють всередину організму і володіють алергічними або токсико-алергічними властивостями». Підкреслюють, що етіологічний фактор в даному випадку проникає в шкіру гематогенним шляхом, а головну роль відводять екзогенним токсинам. Однак зазначають, що існує також ендогенна причина токсидермій, а саме «аутоінтоксикація незвичайними продуктами обміну, що з'являються в організмі внаслідок порушення функції шлунково-кишкового тракту, печінки, нирок».
Під терміном бактеріальна токсикодермія мали на увазі гостре чи хронічне подразнення або запалення шкірних покривів, що виникає під впливом бактеріальних дерматотропних токсинів бактерій, що викликають нефродисбактеріоз та/або пієлонефрит і СХБІ. Тобто головним вогнищем формування бактеріальних токсинів, що подразнюють та уражають шкіру, у 100% випадків таких захворювань були нирки. Треба зазначити, що поряд з вогнищем у нирках, суттєве значення у виникненні токсикодермій мали ще два вогнища хронічної бактеріальної інфекції. Одне із них знаходилося в носоглотці, було пов’язане первинно з золотистим стафілококом та виявлялося у 100 % хворих на СХБІ з ураженням шкіри. Іншим супутнім до походження бактеріальних токсикодермій вогнищем, у якому продукувалися дерматотропні токсини, був кишківник особливо у випадках виникнення в ньому дисбактеріозу, що частіше виявлялося та мало важливе значення у дітей грудного віку та перших 3-5 років життя.
Бактеріальні токсикодермії могли бути додатково спровоковані та посилені також зовнішніми чинниками (тригерні фактори) токсичного або токсико-алергічного характеру, які проникали в організм через травний тракт, дихальні шляхи або при парентеральному (внутрішньовенному, внутрішньом’язовому або підшкірному) введенні. Токсикодермія відрізняється від інших дерматитів тим, що провокуючий агент потрапляв не безпосередньо на шкіру, а проникав в неї разом з потоком крові – тобто гематогенним шляхом. Не виключений також лімфогенний шлях поширення бактеріальних токсинів. Тригерні фактори, що зовнішньо дають формально головний або додатковий поштовх клінічній маніфестації захворювання, зазвичай, запускають вже сформований, але до пори латентний «дрімаючій» процес ураження шкіри токсинами бактеріального походження, сенсибілізація до яких могла накопичуватися роками.
Бактеріальні токсикодермії були одними із найбільш частих проявів СХБІ і відмічали їх більш ніж у третини дорослих та майже у полови дітей. Якщо кажуть, що язик - це дзеркало шлунково-кишкового тракту, то склалося таке чітке враження, що шкіра – дзеркало нирок. Клінічні дерматологічні діагнози, які встановлювали хворим на СХБІ, включали такі частіше нозологічно відокремлені захворювання, як власно токсикодермії (плямиста, папульозна, вузлувата, везикульозна, пустульозна, бульозна), атопічний дерматит та інші варіанти дерматитів (нейродерміт, контактний дерматит, алергічний дерматит, себорейний дерматит), еритеми (мігруюча, кільцеподібна, багатоформна ексудативна), кропивниця, локальний асиметричний набряк Квінке зазвичай на обличчі (губи, повіки), екзема, псоріаз, бешиха. Тобто усі ці діагностично сталі захворювання розглядали як різні клінічні варіанти бактеріальної токсикодермії, яка виникла на тлі нефродисбактеріозу/пієлонефриту та була лише одним із проявів СХБІ. Такий незвичайний погляд на природу цих захворювань шкіри, багато з яких зазвичай вважають генетично детермінованими та/або спадковими, тобто, читай – невиліковними, дозволив змінити стратегію та тактику їх лікування. А саме: лікували не шкіру та алергію, а СХБІ, який призводив до ушкодження різних органів та систем організму, у тому числі - і шкіри. Такий підхід до лікування цих різноманітних уражень шкіри та лікування їх максимально без використання протиалергійних, гормональних препаратів та антибіотиків з призначенням бактеріальних вакцин дозволяв досягти ефективності лікування у дітей зокрема таких захворювань, як атопічний дерматит, екзема, псоріаз на рівні 80-100 %. Але зазвичай тільки у дітей. У дорослих, які прожили з цими діагнозами майже все життя, найбільше, на що можна було розраховувати, так це досягнення більш менш стійкої ремісії. Хоча у випадках початку лікування у дорослих зі стажем захворювання до 3-х років результати також були значно кращими. Детальніше результати лікування будуть розглянуті у наступних повідомленнях про СХБІ. А зараз приведемо один із багатьох обнадійливих прикладів такого успішного лікування.
Приклад 8.
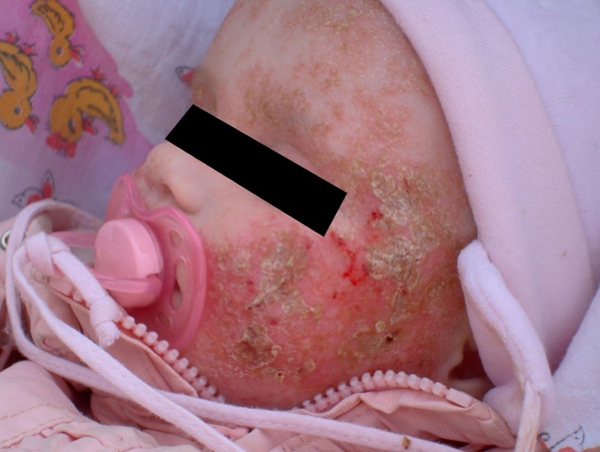
Дитина Марічка, батьки якої звернулися в клініку в грудні 2008 року, коли дитині було 3 місяці, зі скаргами на неоформлені випорожнення зеленого кольору зі слизом, поганий сон, притиснення ніжок до живота, крики та занепокоєння дитини. З калу, носу і глотки були виділені ідентичні штами Staphylococcus aureus. У зв'язку з відсутністю системних проявів стафілококової інфекції, а також з урахуванням грудного віку дитини і побажань батьків було проведено тільки місцеве лікування носоглотки і дисбактеріозу кишківника, після чого стан дитини клінічно покращився. Але вже найближчим часом у віці 6 місяців спочатку на шкірі обличчя, а потім дуже швидко суцільно на тулубі та кінцівках з'явився висип, який був верифікован фахівцями-дерматологами як атопічний дерматит (генетично детермінований – спадковий) з елементами мокрої екземи (див. фото 1). Дитині було призначене відповідне до існуючого протоколу лікування з використанням кортикостероїдних препаратів та антибіотиків, але до початку призначеного лікування батьки Марічки знову звернулися до нашої клініки.
При бактеріологічному дослідженні повторно з носоглотки і калу, та додатково з різних уражених ділянок шкіри, а також з сечі були виділені ідентичні штами Staphylococcus aureus. Рівень загального IgE підвищився з 2 до 110 МО/мл (вікова норма - до 10 МО/мл). Були проведені 2 курси імунізації стафілококовою автовакциною (кожен - по 10 ін'єкцій). Протягом найближчих від початку лікування 6 місяців відзначена позитивна клінічна динаміка: шкіра повністю очистилася від елементів висипу (див. фото 2). Рівень загального IgE знизився до 19 МО/мл. На протязі наступних 11 років спостереження (25.09.2020 р. дитині виповнилося 12 років) рецидивів атопічного дерматиту більше не було, шкіра дитини залишається гладенькою як пасхальне яєчко. Дієти не дотримувалась, обмежень в харчуванні і режимі життя не було. Майже професійно вже тривалий час успішно займається спортом на тенісному корті.
Раніше були розглянуті такі типові алгічні стани як артралгії, спонділалгії та міалгії, включаючи фіброміалгічний синдром, які відносили до клінічних проявів СХБІ, викликаних артроміотропними токсинами. Окремо треба зупинитися на такому тяжкому захворюванні як реактивні артрити (РеА), які теж розглядали як наслідок дії артроміотропних токсинів бактерій у хворих на нефродисбактеріоз та пієлонефрит.
В даний час до РеА відносять запальні негнійні захворювання суглобів, що розвиваються внаслідок імунних порушень після гострих кишкової інфекції (у 1,5-4 % випадків) і частіше, за сталими уявленнями, викликані токсинами таких ентеробактерій як Yersinia, Salmonella та Shigella, а також урогенітальних інфекцій, що передаються статевим шляхом (1-3 %), серед яких 80 % випадків пов’язують із Chlamydia trachomatis, пояснюючи
це «пандемією хламідіозу у світі». В етіологічному плані РеА пов’язують ще з деякими інфекціями респіраторного тракту, а саме з Mycoplasma pneumoniae і Chlamydia pneumoniaе,
Фото 1.
Фото 2.
які начебто також можуть бути причинами розвитку РеА. Таке твердження виглядає щонайменше дивним. З огляду на наш 25-річний досвід клінічного спостереження за пацієнтами з цими суто легеневими інфекціями, вони жодного разу не викликали реактивних артритів. Окремо треба наголосити, що так само як і легеневі, нешкідливими є і урогенітальні мікоплазми та уреаплазми. Враховуючи клінічний досвід за той же період спостереження та лікування пацієнтів з урогенітальними запальними захворюваннями, можна стверджувати, що ці статеві інфекції взагалі є сапрофітною флорою і ніколи, ні у кого і ні при яких обставинах не викликають запальних урогенітальних захворювань і тим більше не можуть бути тригерним фактором виникнення РеА, про що повідомляють деякі джерела.
До збудників інфекцій дихальних шляхів, які, за деякими повідомленнями, також можуть викликати РеА, чомусь, скоріше помилково, віднесено навіть Klebsiella pneumoniae. Мабуть тому, що ця типова кишкова бактерія, яка довічно живе у кишківнику кожної людини і саме там залишається сапрофітною, історично має назву клебсієла пневмонія. При зміні території перебування на усіх інших слизових оболонках, включаючи дихальну систему, клебсієла може викликати тяжкі гнійні запальні процеси. Реактивні зміни негнійного характеру у суглобах, пов’язані з клебсієлою, цілком можливі, але виключно у випадках її персистування у нирках при нефродисбактеріозі/пієлонефриті.
Ані в доступній медичній літературі, ані у мережі інтернет, ані у попередніх та сучасних класифікаціях реактивних артритів, ані у матеріалах ВООЗ повідомлень про те, що вогнище первинної інфекції, яка є пусковим фактором вторинного розвитку реактивних артритів, може знаходитися у нирках не знайдено. Не знайдено також ані пари з вуст про те, що збудниками РеА можуть виступати звичайні природньо симбіотичні та сапрофітні ентеробактерії та ентерококи, що довічно живуть в кишківнику людини, а також патогенні стафілококи та стрептококи, у випадках утворення цими бактеріями вогнища хронічної бактеріальної інфекції у нирках.
Треба також відзначити наступне. Із літератури, стосовно РеА, відомо, що неодноразово були виявлені факти гострого ураження кишківника та/або сечостатевих шляхів не тільки як первинних по відношенню до РеА, але з можливістю розвитку одночасно з ним і навіть після появи ураження суглобів. Це порушує «встановлені» причинно-наслідкові зв'язки та робить назагал існуюче твердження, що РеА є наслідком гострих статевих та кишкових інфекцій, просто нелогічним. І ще одна дивна обставина. Не може в етіологічному плані принципово відрізнятися збудниками одне і теж саме захворювання у дітей та дорослих, як скажімо, гайморит, або бронхіальна астма, або пієлонефрит, або усі інші людські біди, що мають інфекційне походження. Тоді де ж та хламідійна етіологія походження РеА у дітей, які так само хворіють на РеА, що є пусковим фактором начебто 80 % захворювань у дорослих? У дітей, які ще навіть сенсу слів статеве життя не усвідомлюють, а вже бачиш – хворіють?
На протязі останніх 11 років (з 2009 р.) під нашим спостереженням і лікуванням знаходилися 770/4500 (17,1 %) хворих з СХБІ на тлі нефродисбактеріозу та/або пієлонефриту з домінуючим у клінічній картині захворювання реактивним негнійним запаленням суглобів. Дорослих було 540/2340 (23 %), дітей шкільного віку – 157/870 (18 %) та у віці від 3-х до 7 років – 73/750 (9,7 %). Зазвичай, діагнози ураження суглобів були встановлені ще на попередніх етапах обстеження та лікування: реактивного артриту – у 560/770 (72,7 %) випадках (ще у 70/770 або 9,1 % випадках діагноз РеА був первинно встановлений в нашій клініці), ревматоїдного артриту (РА) – 70 (9,1 %), включаючи ювенільний РА у 9 дітей (1,1 %), а також артритів на тлі подагри – 45/770 (5,8 %) випадків, псоріазу – 15/770 (1,9 %) та ураження суглобів, що відбувалося на тлі бореліозу (хвороби Лайма) – у 10 хворих (1,3 %), що назагал становило також 70/770 (9,1 %) випадків. Синдром Рейтера на тлі нефродисбактеріозу розвивався у поодиноких випадках – всього у 12/770 (1,5 %) хворих. Зміни шкіри та слизових оболонок при синдромі Рейтера, які протікали у вигляді кератодермії та безболісних виразок на статевих органах, розглядали як класичну бактеріальну токсикодермію, яку дуже часто виявляли при нефродисбактеріозі навіть без ураження суглобів.
Серед пацієнтів з РеА переважали дорослі (540/770 або 70,1 %), хоча і дітей було чимало – майже третина (230/770 або 29,9 %). У 747/770 (97 %) випадках захворювання суглобів було хронічним і тривало більше 1 року. Треба ще раз наголосити, що у всіх 770 пацієнтів з ураженням суглобів, які знаходилися під спостереженням, реактивні артрити розвинулися не після гострих статевих та/або кишкових інфекцій, як зазвичай повідомляють при встановлені цього діагнозу. Крім того, у всіх дорослих було виключено (методами ІФА та за потреби - ПЛР) хронічне інфікування статевим хламідіозом. РеА розвивалися на тлі хронічної бактеріальної інфекції в нирках - нефродисбактеріозу, рідше – маніфестного пієлонефриту, що призвело до розвитку СХБІ з домінуючим в даних випадках ураженням суглобів, яким хибно надавали інші діагнози.
У хворих з подагрою, псоріазом та хворобою Лайма лікування артритів бактеріальними вакцинами з досягненням швидкого та відносно стабільного позитивного клінічного результату без використання або з припиненням прийому препаратів, які зазвичай призначають хворим з такими діагнозами, ex juvantibus підтверджувало первинну роль в ураженні суглобів токсинів бактерій, що викликали нефродисбактеріоз та/або пієлонефрит. При цьому нерідко виникала така парадоксальна ситуація, коли у недужих начебто з подагричним артритом рівень сечової кислоти знижувався чи залишався у межах норми, а запалення суглобів продовжувало прогресувати. І навпаки: при значно підвищеному рівні сечової кислоти після початку лікування бактеріальною вакциною біль у суглобах повністю минав. Приклад ефективного лікування бактеріальними вакцинами хворого на подагру, у якого поліартрит 10 років не піддавався стандартному у таких випадках лікуванню, у зв’язку з чим вже збиралися призначати терапію цитостатичними препаратами, вже наводили раніше (див. Приклад 1 у Повідомленні 1). Наведемо ще два приклади: успішного лікування молодого чоловіка бактеріальними вакцинами, у якого реактивний артрит на протязі 2 років «протокольної» терапії здавався нездоланним, а також ревматоїдного артриту у малої дитини, у кожному із яких все, що відбувалося, мало великі шанси закінчитися повною інвалідізацією пацієнтів.
Приклад 9.
Чоловік 35 років, звернувся до клініки навесні 2017 р. Хворіє 2 роки з дуже сильним болем у несиметричних суглобах верхніх та нижніх кінцівок з періодичною їх деформацією. Був встановлений діагноз реактивного артриту без визначення етіологічного фактору: напередодні виникнення болю в суглобах на протязі 6 місяців ніяких епізодів гострих інфекційних захворювань сечостатевої системи та кишківника не було. Майже безперервно на протязі усього захворювання приймає нестероїдні протизапальні препарати (НПЗП) у середньо-високому дозуванні, а неодноразові спроби відміни препаратів та навіть зменшення дози призводили до загострення РеА з поверненням болю та приєднанням ураження нових суглобів. Додатково при огляді у клініці пацієнт поскаржився на постійну субфебрільну температуру, слабкість, зниження життєвої енергії, головний біль, періодичне запаморочення, підвищену пітливість, зниження толерантності до фізичних та спортивних навантажень, довготривалу гіпохромну анемію. Вже майже рік не працює, кульгає, ходить з паличкою. Лікар рекомендував оформлювати групу інвалідності, бо «прогноз невтішний». Із анамнезу також встановлено, що майже 7 років тому переніс дебют гострого пієлонефриту, який до теперішнього часу залишався у повній довготривалій клінічній латенції, моніторинг загального аналізу сечі не проводив.
При обстеженні у клініці в сечі було виявлено помірковану протеїнурію (0,066 г/л), лейкоцитурію (8-10 у п/з), одиничні змінені еритроцити та зернисті циліндри, бактеріурію. Бактеріологічним дослідженням теплої сечі (три дні поспіль виділяли ідентичну культуру Enterococcus faecalis) був підтверджений діагноз нефродисбактеріозу (з дебютом пієлонефриту в віддаленому анамнезі) з розвитком СХБІ і домінуючою картиною вторинного реактивного артриту. Був призначений цикл лікування (із двох курсів по 10 ін’єкцій кожен з інтервалом між курсами в 1 місяць) бактеріальними двовалентними ешеріхіозно-ентерококовими аутовакцинами, який дав найближчі позитивні клінічні результати. Була суттєво зменшена доза НПЗП (без погіршення загального стану та рецидиву артриту), майже зникли болі у суглобах, повернувся до роботи. За 2 місяці після завершення першого циклу вакцинації виник рецидив РеА, але з меншим больовим навантаженням. Після контрольного бакпосіву сечі (виділена культура E.coli) був призначений другий цикл вакцинації. На даний час (вересень 2020 р.) пройшов 5 циклів вакцинації, НПЗП вже майже 2 роки взагалі не застосовує, скарг не має, працює, регулярно тренується у спортзалі. Рецидивів РеА вже більше року не було. Залишається під наглядом та проходить періодичне бактеріологічне обстеження сечі.
Приклад 10.
Хлопчик 3 років, назвемо його Андрійком, хворів вже майже рік. Батьки дитини звернулися у клініку Вітацелл на початку 2006 року. Діагноз, який був встановлений дитині за місцем мешкання у одному із південних обласних центрів України, для батьків звучав як вирок: ювенільний ревматоїдний артрит. При генетичному обстежені дитини був виявлений антиген HLA-B27, що, з міркувань місцевих лікарів, пояснювало важкий перебіг захворювання та значно погіршувало його прогноз. Були уражені переважно суглоби нижніх кінцівок, дитина вже 4 місяці не ходила: до кабінету батько заніс хлопчика на руках. З самого початку захворювання перебував на глюкокортикостероїдній терапії в середньо-високому дозуванні, але запальний процес в суглобах майже не зупинявся і з кожним наступним рецидивом ситуація тільки погіршувалася. Батькам обґрунтовано пояснили, що треба готуватися до гіршого і дитина, скоріше за все, у найближчий перспективі стане повним інвалідом, бо «дуже рано все почалося». Із додаткових симптомів при огляді дитини в Києві виявили затяжний субфебрилітет, підвищену пітливість, з’ясували із анамнезу схильність до частих простудних захворювань з розвитком 6 місяців тому гострого гаймориту, тривале зниження рівня еритроцитів та лейкоцитів, періодичну висипку на шкірі по типу рецидивної кропивниці та атопічного дерматиту. Батьки згадали, що часом у дитини помічали часте сечовипускання, яке ні вони, ні лікарі не пов’язували з ураженням суглобів.
На підставі бактеріологічного дослідження сечі (три дні поспіль) з виділенням по три штами E.coli та Enterococcus faecalis, а також мазків із носу та горла (виділений St.aureus) був встановлений діагноз: нефродисбактеріоз (домінуюче еширіхіозно-ентерококовий), локально безсимптомний з розвитком синдрому хронічної бактеріальної інтоксикації з домінуючим вторинним реактивним артритом токсичної етіології та супутня хронічна стафілококова інфекція носоглотки з частими простудними захворюваннями та рецидивним риносинуситом. Гормонозалежна форма ювенільного ревматоїдного артриту? Був призначений курс послідовного лікування трьома бактеріальними вакцинами: спочатку стафілококовою - із 7 ін’єкцій, потім ешеріхіозно-ентерококовою з 3 аутоштамами E.coli та 3-ма - Enterococcus faecalis, ще 10 ін’єкцій та на завершення - полівалентною вакциною, виготовленою із власних штамів бактерій, також із 10 ін’єкцій. Вже під час першого циклу лікування дитина встала на ноги, почала самостійно ходити, зник субфебрилітет, припинили давати преднізолон. За два наступних роки було проведено назагал 3 цикли лікування бактеріальними вакцинами: рецидиви запалення в суглобах припинилися, дитина повністю одужала. Катамнестичне спостереження тривало 10 років (аж до 2015 р. - потім зв’язок перервався), рецидивів артриту більше не було. На неодноразові звернення до матусі хлопчика з проханням виступити на одному із телевізійних каналів та розповісти історію чудового одужання дитини, щоб дати надію іншим батькам таких дітей із «ревматоїдними артритами», вона беззастережно відмовлялася, бо, як казала, «боюся наврочити».
Дуже часто наголошують, що в реальній практиці термін РеА помилково використовують набагато ширше і включають до нього артрити іншої етіології: після перенесеної вірусної інфекції, поствакцинальні артрити, постстрептококовий артрит і деякі інші. Тому в нашому випадку або мова йде про невідомий раніше варіант реактивного (стерильного) ураження суглобів на тлі хронічної інфекції нирок (нефродисбактеріоз та пієлонефрит), або просто хворі з діагнозами вторинних реактивних негнійних артритів незалежно від першопричини не були раніше досліджені бактеріологічно на наявність у них бактерій у нирках.
Стан не визначений: діагноз та лікування багатьох пацієнтів з РеА, а можливо - і з РА та іншими варіантами негнійних артритів, не відповідають справжній етіологічній причині їх захворювання. Незважаючи на майже постійне, інколи - пожиттєве використання різних препаратів, більшість з яких мають шкідливі побічні дії, ураження суглобів зазвичай тільки прогресує, майже не реагуючи на намагання та спроби їх зупинити, з високим ризиком інвалідизації таких хворих.
Серед клінічних симптомів СХБІ, викладених у таблиці 1 (див. Повідомлення 2), залишилися ще нерозглянутими ураження, викликані офтальмотропними токсинами: кон’юнктивіти, увеїти, неврит зорового нерву та диплопія.
Інфекційне ураження слизової оболонки ока (кон’юнктиви) може бути вірусної, бактеріальної або токсичної природи. Найбільш поширені та вивчені вірусні та бактеріальні (гнійні) кон’юнктивіти. Кон'юнктивіт, викликаний впливом токсичних речовин екзогенного походження, носить назву токсичний кон'юнктивіт. Розвиток такого виду кон'юнктивіту відбувається в результаті характерної реакції організму людини на вплив певних хімічних речовин (наприклад, лаків, різних хімічних реактивів, промислових парів, фарби і багато іншого). Відомості про токсичний кон’юнктивіт ендогенного походження, який виникає за рахунок ураження ока токсинами бактерій (при наявності в організмі вогнища хронічної бактеріальної інфекції в нирках), в доступній медичній літературі не знайдені.
Під нашим спостереженням знаходилися 211/2340 (9 %) дорослих та 18/870 (2 %) дітей шкільного віку з СХБІ, у яких спостерігали ураження кон’юнктиви токсичного ендогенного походження. Кон’юнктивіти носили не гнійний характер, але і вірусна природа їх виникнення при лабораторному обстежені теж була виключена. Ми вже згадували вище, при розгляді клінічних проявів дії дерматотропних токсинів, що такі клінічні симптоми токсичних подразнень слизових оболонок очей як постійне, а інколи нападоподібне відчуття печіння та «піску» в очах, що викликало помірковану або нездоланну сльозотечу, відмічали більше половини дорослих (1334/2340 або 57 %) та навіть 70/870 або 8 % дітей шкільного віку. У випадках прогресування токсичного ураження слизових оболонок очей виникав токсичний кон’юнктивіт (зазвичай були вражені обидва ока) з набряком повік, набряком і гіперемією кон'юнктиви, світлобоязню, подальшим посиленням сльозотечі, почервонінням білка очей, сверблячкою очей, а іноді - болем в очах.
Серед увеїтів (запалення судинної оболонки ока) найбільш поширена інфекційна природа їх виникнення, а саме - вірусної етіології. Зазвичай вражаються обидва ока. Серед найбільш поширених є віруси герпесу: цитомегаловірус, вірус Епштейна-Барр, вірус простого герпесу і лише інколи - вірус вітряної віспи. Крім вірусів герпесу увеїти можуть викликати токсоплазмоз, туберкульоз; у більш рідких поодиноких випадках ураження зорового тракту можуть зустрічатися при гістоплазмозі, токсокарозі, хворобі Лайма (бореліоз), сифілісі та як казуїстика - при деяких інших інфекційних захворюваннях.
В деяких непоодиноких випадках інфекційну або іншу відому класичну природу увеїтів (аутоімунну, постравматичну та ін.) встановити неможливо – результати адекватного лабораторного обстеження дають негативні результати. Як виявилося, зазвичай такі увеїти мають токсичну природу (ендотоксичний увеїт) і виникають внаслідок ендогенного ураження судин увеального тракту токсинами бактерій, хронічне вогнище яких знаходиться у в нирках. Частина з цих токсинів має відповідну офтальмотропність з вибірковим домінуванням ураження судин зорового тракту.
Під нашим спостереженням знаходилися 24/4500 (0,53 %) пацієнти з СХБІ, у яких був раніше встановлений діагноз увеїту невизначеної етіології. Дітей у віці від 3-х до 7 років було 3/750 (0,4 %), від 7 до 14 років – 7/870 (0,8 %) та дорослих – 14/2340 (0,6 %). Частіше були вражені обидва ока (у 19/24 або 79,2 % пацієнтів) та майже у всіх випадках (23/24 або 95,8 %) це був задній увеїт з ураженням хоріоідеї, сітківки та/або зорового нерву, у тому числі у 3 дорослих – з домінуванням застійних дисків зорових нервів. Хоча, можливо, така вибірковість ураження пояснювалася вибірковістю обстежених пацієнтів (тільки ті, що звернулися до інфекціоніста у клініку) та обмеженою кількістю спостережень пацієнтів з ураженням увеального тракту. Ще 5/2340 (0,57 %) дорослих, у яких в клініці був виявлений СХБІ, звернулися з діагнозом ретробульбарний неврит (або неврит II черепного зорового нерву при непошкодженому соску нерву). У хворих під час попередніх офтальмологічних спостережень були виключені демієлінізуючі захворювання ЦНС, пухлини головного мозку, запалення вмісту очниці, синусити та інші відомі етіологічні фактори цього досить рідкого патологічного стану, частота виникнення якого за різними повідомленнями оцінюється від 1 до 5 випадків на 100 тис. Патогенез невриту очного нерву залишається напевно невстановленим, хоча з 2000-х років все більше говорять про руйнування аксонів і нейронів як первинних чинників розвитку процесу, але причина цього нейродегенеративного ушкодження досі не з’ясовна.
Тривалість захворювань, етіологія яких весь час попередніх спостережень залишалася невизначеною, складала від 5-6 місяців до 7-8 років. Незважаючи на постійне фахове лікування за існуючими для таких випадків міжнародними протоколами стан очей помітно та стабільно не поліпшувався, а гострота зору постійно знижувалася, як у наступному прикладі.
Приклад 11.
Пацієнтка Т., 18 років. Звернулися в клініку разом з батьком, який опікав доньку як малу дитину, 10.09.2014 р. з діагнозом направлення: застійні диски зорових нервів обох очей зі зниженням зору (VOD - 0,4; VOS - 0,3). Попередні курси звичайного у таких випадках лікування, які проводили у декількох офтальмологічних клініках Києва, тривали 2 роки 9 місяців з практично нульовим результатом – застійні явища тільки посилювалися, а гострота зору знижувалася. Етіологія цих застійних дисків залишалася не верифікованою. Пройшла в клініці додаткове обстеження на герпесвірусні інфекції – активних форм не виявлено; на стан імунітету та ревмопроби – норма; були відсутні серологічні ознаки аутоімунно-системних захворювань. Спочатку було запідозрено, а потім і підтверджено при бактеріологічному дослідженні сечі виділенням 3-х урінокультур Enterococcus faecalis діагноз урогенітального дисбактеріозу з дебютом циститу в найближчому анамнезі (в березні 2014 г.) та розвитком нефродисбактеріозу, який протікав з проявами синдрому хронічної бактеріальної інтоксикації та, за даними діагностичної системи Токсикон, з ендотоксикозом, токсемією середнього ступеня резорбтивного ґенезу, а також вторинною гіпохромною анемією, епізодами цефалгій і переважною астеновегетативною симптоматикою. Так уперше у нашій практиці було встановлено, що застійні диски зорових нервів, утрата гостроти зору, а так само зміни на МРТ і вазограмі судин головного мозку можуть мати токсичну етіологію, асоційовану з ендотоксикозом бактеріального походження.
Був проведений перший курс лікування бактеріальною аутовакциною з додаванням 3-х аутоштамів Enterococcus faecalis із 10 підшкірних ін'єкцій. Прийшла на контрольний огляд через 2 місяці після закінчення вакцинації (15.12.2014 р.). Виявилося, що вже через 15 днів після початку лікування гострота зору підвищилася майже до норми - 90-100% і повністю зникли візуальні ознаки набряків диска зорового нерву лівого ока, а потім через 2,5 місяці після початку лікування - і правого ока. Крім того, за даними ультразвукового обстеження судин головного мозку, за 2,5 місяці повністю відновився симетричний кровоплин по середнім мозковим артеріям і відзначена позитивна динаміка в порушеному венозному відтоку з порожнини черепа. Через 3 місяці після закінчення 1-го курсу були проведені ще два курси вакцинації: 2-й курс імунізації ешеріхіозно-ентерококовою вакциною з додаванням на цей раз 3-х нових аутоштамів Enterococcus faecalis та 2-х - E.coli, що були виділенні при контрольному обстеженні теплої сечі – також із 10 ін'єкцій, а потім ще 3-й курс - бактеріальною аутовакциною, виготовленою із аутоштамів бактерій, також із 10 ін’єкцій. Протягом наступних 6 років катамнестичних спостереження рецидивів втрати зору (зберігається 100% зір на обидва ока), так само як і циститу та бактеріурії більше не було.
У 7/2340 (0,3 %) дорослих без проявів увеїту та/або невриту зорового нерву виникала тимчасова минуща диплопія, механізм виникнення якої, окрім того, що вона зрозуміло носила токсичний характер, залишився не з’ясованим. Можливо, як і при ботулізмі, мало місце токсичне ураження ядер III, IV та VI (відвідний) черепних нервів, але на відміну від ботулотоксину дія токсинів бактерій при нефродисбактеріозі/пієлонефриті носила зворотній характер та зникала після зменшення ендотоксикозу, яким був обумовлений СХБІ. Можна припускати, що при СХБІ має також місце не тільки встановлене токсичне ураження II (зорового) чи V (трійчастого) черепних нервів чи ймовірне пошкодження III (окорухового), IV (блокового) та VI (відвідного), але і інших черепних нервів, наприклад, X (блукаючого) чи I (нюхового) нервів з появою відповідної клінічної симптоматики. Тим більше, що з великого клінічного переліку вегетативних невропатій при СХБІ, які вважали периферичними за рахунок впливу нейровазотропних токсинів та відмічали у переважної більшості дорослих (від 65 % до 94 %) та нерідко у дітей шкільного віку, певна частина з них могла мати саме центральне походження (напр., серцевий ритм, виділення залоз внутрішньої секреції). А скарги на порушення нюху від хворих на СХБІ доводилося чути неодноразово, хоча причина їх виникнення залишалася не зрозумілою. Але це питання потребує окремого додаткового вивчення.
На завершення обговорення клінічних проявів СХБІ треба зупинитися ще на одній цікавій та важливий обставині. Майже у 100 % дітей та у 50-70 % дорослих з СХБІ виявляли хронічну стафілококову інфекцію, первинне вогнище якої знаходилося у носоглотці. Це привносило у клінічну картину захворювання такі типові для цієї інфекції клінічні симптоми, як схильність до частих простудних захворювань, хронічний тонзиліт з рецидивними ангінами, фарингіт з частим болем у горлі, запальні процеси у додаткових пазухах носу, вухах, очах, аденоїди у дітей та поступовий розвиток на тлі хронічного запалення слизових оболонок додаткових пазух носу кіст та поліпів частіше верхньощелепної (гайморової) пазухи у дорослих, збільшення та хворобливість лімфатичних вузлів лімфоглоткового кільця, «підліткову» піодермію, фурункульоз та ін. Саме вогнищем хронічної стафілококової інфекції у носоглотці можна було пояснити виникнення таких симптомів як фарингіт, біль у горлі і збільшення лімфатичних вузлів носоглоткового кільця, на які дуже часто посилалися раніше при вивченні клінічної картини СХУ, але поява яких залишалася невстановленою.
Окремо також треба зазначити, що розвиток СХБІ не залежав від наявності запального процесу у нирках. Так серед 2340 дорослих з діагнозом нефродисбактеріоз з розвитком СХБІ клінічні згадки та лабораторне і УЗД підтвердження пієлонефриту мали на момент звернення у клініку тільки 281/2340 (12 %) пацієнтів, а серед 2160 дітей – 173 (8 %). Між тим, ще у 585/2340 (25 %) дорослих та 411/2160 (19 %) дітей незважаючи на відсутність у них будь-яких даних з анамнезу та клінічних проявів хронічного пієлонефриту, в загальних аналізах сечі були вперше встановлені мікроскопічні ознаки латентного формування хронічного уповільненого запального процесу в нирках з різним рівнем підвищення білку, лейкоцитів, появою циліндрів та бактерій, рідше - еритроцитів. Тобто у 63% дорослих пацієнтів та 73 % дітей на момент встановлення їм діагнозу СХБІ в них існував нефродисбактеріоз у «чистому» вигляді без усяких ознак запального процесу в нирках.
В результаті катамнестичного спостереження за 700 пацієнтами (дорослих – 420, дітей – 280) з діагнозом нефродисбактеріозу, які або не проходили взагалі, або пройшли лише 1-2 курси лікування бактеріальними аутовакцинами, не досягнувши повної санації вогнища в нирках, було встановлено наступне. Більш ніж у третині випадків (у 157/420 або 37,4 % дорослих та 110/280 або 39,2 % дітей) розвинувся дебют пієлонефриту у терміни від декількох годин (казуїстичні випадки) до декількох років (інколи – 8-10 років) після первинного клінічного встановлення та/або бактеріологічного підтвердження у них діагнозу нефродисбактеріозу.
З огляду на таке, мабуть треба визнати, що «гострих пієлонефритів» взагалі майже не існує. У випадках виникнення «гострого» запалення в нирках переважно завжди (за винятком первинно гематогенного ураження нирок у септичних хворих) має місце первинний дебют хронічного уповільненого пієлонефриту із зазвичай довготривалим латентним формуванням на тлі нефродисбактеріозу. Тобто спочатку відбувається клінічно безсимптомне заселення нирок висхідним шляхом переважно бактеріями кишкової групи, ентерококами та стафілококами. Така собі тиха довготривала мікробна повзуча окупація слизових оболонок переважно чашково-мискової та канальцевої системи нирок з розвитком спочатку віддалених симптомів загальної інтоксикації (СХБІ), а потім внаслідок дії різноманітних несприятливих тригерних факторів - виникненням ознак локального запального процесу, тобто класичного пієлонефриту. Одним із частих провокуючих факторів розвитку нефродисбактеріозу у дорослих була сечокам'яна хвороба. Клінічні ознаки хронічного циститу, який розглядали як додаткову браму висхідної інфекції, на момент звернення на консультацію у клініку або згадки з анамнезу про перенесенні раніше епізоди циститу мали майже 39 % (912/2340) дорослих та майже 35 % (755/2160) дітей.
Незважаючи на велику кількість симптомів, з якими міг протікати СХБІ, у деяких випадках можна було казати про моносимптомний СХБІ, який мав не просто домінуючий, а майже тільки один прояв: або тільки головний біль, або тригемініт, або реактивний артрит, або алопецію, або затяжний субфебрилітет, або ізольовано підвищену ШОЕ чи лейкопенію та ще безліч подібних або. Цю характерну обставину треба було обов’язково враховувати при огляді недужих з цим клінічно строкатим синдромом хронічної бактеріальної інтоксикації.
Ще не кінець. Далі ще трохи буде.
Висновки.
1. Одними з головних клінічних проявів дії дерматотропних токсинів у хворих на СХБІ було дуже часте пряме ураження шкіри з появою різноманітних варіантів дерматитів, які, незважаючи на різні назви, поєднувала одна загальна патогенетична причина: вони були викликані бактеріальними токсинами дерматологічної спрямованості. Бактеріальні токсикодермії частіше спостерігали у дітей: у віці до 3-х років – у 222/540 (41 %) випадках, у віці від 3-х до 7 років – у 398/750 (53 %), від 7 до 14 років – у 392/870 (45 %) та у 889/2340 (38 %) дорослих. Ураження шкіри майже завжди було поєднаним з іншими симптомами СХБІ, хоча нерідко помітно домінувало у клінічній картині захворювання.
2. Клінічні дерматологічні діагнози, які встановлювали хворим на СХБІ, включали такі частіше нозологічно відокремлені захворювання, як власно токсикодермії (зокрема плямиста, папульозна, везикульозна, пустульозна, бульозна), атопічний дерматит та інші варіанти дерматитів (зокрема нейродерміт, алергічний дерматит, себорейний дерматит), ерітеми (мігруюча, кільцеподібна, багатоформна ексудативна), кропивниця, локальний асиметричний набряк Квінке зазвичай на обличчі (губи, повіки), екзема, псоріаз. Тобто усі ці діагностично сталі захворювання розглядали як різні клінічні варіанти бактеріальної токсикодермії, яка виникла на тлі нефродисбактеріозу/пієлонефриту та була лише одним із проявів СХБІ, що давало можливість змінити стратегію та тактику їх лікування. А саме: лікували не шкіру та алергію, а СХБІ, який призводив до ушкодження різних органів та систем організму, у тому числі - шкіри, що дозволяло досягти ефективності лікування у дітей бактеріальних токсикодермій, зокрема таких захворювань, як атопічний дерматит та екзема, на рівні 80-100 %.
3. До клінічних проявів СХБІ, викликаних артроміотропними токсинами, відносили реактивні артрити (РеА), які спостерігали у 770/4500 (17,1 %) хворих на СХБІ. Дорослих було 540/2340 (23 %), дітей шкільного віку – 157/870 (18 %) та у віці від 3-х до 7 років – 73/750 (9,7 %). За нашими спостереженнями та результатами лікування пацієнтів з домінуючим у клінічній картині захворювання реактивним запаленням суглобів, цей патологічний стан не був пов’язаний з попередньо перенесеними гострими кишковими та статевими інфекціями, а також із хронічним статевим хламідіозом, які й досі вважають головним чинником виникнення РеА. Більш того, було також встановлено, що РеА на тлі СХБІ є навіть серед хворих дітей та дорослих з такими діагнозами як ревматоїдний артрит (під нашим наглядом було 70/770 або 9,1 % таких пацієнтів, включаючи ювенільний РА у 9 дітей або 1,1 %), а також подагричний артрит - 45/770 (5,8 %) випадків, псоріатичний артрит – 15/770 (1,9 %) та ураження суглобів, що відбувалося начебто на тлі бореліозу (хвороби Лайма) – у 10 хворих (1,3 %), що назагал становило також 9,1 % (70/770). В усіх цих випадках РеА розвивалися на тлі хронічної бактеріальної інфекції в нирках - нефродисбактеріозу, рідше – маніфестного пієлонефриту, що призвело до розвитку СХБІ з домінуючим ураженням суглобів, яким хибно надавали інші діагнози.
4. Частина бактеріальних токсинів при СХБІ мала ще одне певне клінічне направлення дії, яке окреслювали як офтальмотропне. Під нашим спостереженням знаходилися 211/2340 (9 %) дорослих та 18/870 (2 %) дітей шкільного віку з СХБІ, у яких спостерігали токсичний кон’юнктивіт ендогенного походження з набряком повік, набряком і гіперемією кон'юнктиви, світлобоязню, сльозотечою, почервонінням білка очей, сверблячкою очей, а іноді - болем в очах.
5. Бактеріальні токсини при СХБІ могли викликати не тільки ураження кон’юнктиви, але і зорового тракту. Під нашим спостереженням знаходилися 24/4500 (0,53 %) пацієнти з СХБІ, у яких після виключення вірусної, бактеріальної, аутоімунної та ін. природи захворювання був встановлений діагноз токсичного увеїту ендогенного походження. Дітей у віці від 3-х до 7 років було 3/750 (0,4 %), від 7 до 14 років – 7/870 (0,8 %) та дорослих – 14/2340 (0,6 %). Частіше були вражені обидва ока (у 19/24 або 79,2 % пацієнтів) та майже у всіх випадках (23/24 або 95,8 %) це був задній увеїт з ураженням хоріоідеї, сітківки та/або зорового нерву, у тому числі у 3 дорослих – з домінуванням застійних дисків зорових нервів.
6. До інших поодиноких проявів дії бактеріальних токсинів офтальмотропного направлення відносили ретробульбарний неврит зорового нерву, який спостерігали у 5/2340 (0,57 %) дорослих, у який під час попередніх офтальмологічних спостережень були виключені демієлінізуючі захворювання ЦНС, пухлини головного мозку, запалення вмісту очниці, синусити та інші відомі етіологічні фактори цього досить рідкого патологічного стану, та тимчасова минуча диплопія, яку спостерігали у 7/2340 (0,3 %) дорослих без проявів увеїту та/або невриту зорового нерву, механізм виникнення якої, окрім того, що вона носила токсичний характер, залишився не з’ясованим.
7. Майже у 100 % дітей та у 50-70 % дорослих з СХБІ виявлено хронічну стафілококову інфекцію, первинне вогнище якої знаходилося у носоглотці. Це привносило у клінічну картину захворювання такі типові для цієї інфекції додаткові клінічні симптоми, як схильність до частих простудних захворювань, хронічний тонзиліт з рецидивними ангінами, фарингіт з частим болем у горлі, запальні процеси у придаткових пазухах носу, вухах, очах, аденоїди у дітей та поступовий розвиток у дорослих на тлі хронічного запалення слизових оболонок придаткових пазух носу кіст та поліпів частіше верхньощелепної (гайморової) пазухи, збільшення та хворобливість лімфатичних вузлів лімфоглоткового кільця, «підліткову» піодермію, фурункульоз та ін. Саме вогнищем хронічної стафілококової інфекції у носоглотці можна було пояснити появу таких симптомів як фарингіт, біль у горлі і збільшення лімфатичних вузлів носоглоткового кільця, на які дуже часто посилалися раніше при вивченні клінічної картини СХУ, але поява яких залишалася невстановленою.
8. Розвиток СХБІ не залежав від наявності запального процесу у нирках. Так серед 2340 дорослих з діагнозом нефродисбактеріоз з розвитком СХБІ клінічні згадки та лабораторне і УЗД підтвердження наявності пієлонефриту мали на момент звернення у клініку тільки 281 (12 %) пацієнтів, а серед 2160 дітей – 173 (8 %). Між тим, ще у 585/2340 (25 %) дорослих та 411/2160 (19 %) дітей незважаючи на відсутність у них будь-яких даних з анамнезу та клінічних проявів хронічного пієлонефриту, в загальних аналізах сечі були вперше виявлені мікроскопічні ознаки латентного формування хронічного уповільненого запального процесу в нирках з різним рівнем підвищення білку, лейкоцитів, появою циліндрів та бактерій, рідше - еритроцитів. Таким чином у 63% дорослих пацієнтів та 73 % дітей на момент встановлення їм діагнозу СХБІ в них існував нефродисбактеріоз у «чистому» вигляді без усяких ознак запального процесу в нирках.
9. Встановлено таку характерну клінічну обставину як існування моносимптомного СХБІ, який мав не просто домінуючий, а майже тільки один прояв: або тільки головний біль, або тригемініт, або реактивний артрит, або алопецію, або затяжний субфебрилітет, або ізольовано підвищену ШОЕ (синдромом ізольованого підвищення ШОЕ,) чи лейкопенію та ще безліч подібних або, що треба обов’язково враховувати при діагностиці цього клінічно строкатого синдрому.